A humanidade tenta compreender como melhorar os materiais desde a antiguidade. O homem primitivo percebeu que ao “lascar” as pedras formava novas ferramentas. Usando o fogo notou que era capaz de fundir diversos materiais. Descobriu inclusive que misturando materiais diferentes podiam fabricar as famosas ligas metálicas, com melhores propriedades como dureza, rigidez, tenacidade entre outros.
Aprendemos que ao fundir a areia surgia os vidros, sendo possível a construção de adornos, novas ferramentas, novas formas de construções e… Essa história vai longe!
Com a invenção do microscópio óptico, começamos a descobrir os materiais numa nova escala. Passamos a entender que a microestrutura guarda importantes relações com as propriedades dos materiais. Mas um microscópio óptico tem lá suas limitações. É impossível, por exemplo, ver os átomos de um material com um microscópio óptico…
Neste contexto, a descoberta dos Raios X permitiu um avanço extraordinário na forma como enxergamos os materiais. Sabemos que as propriedades físicas (dureza, rigidez, transparência, condutividade térmica e elétrica, entre outras) dependem da forma como os átomos se arranjam no material. Os raios X permitiram “enxergar” o material numa escala muito menor que o microscópio óptico poderia possibilitar.
Ondas eletromagnéticas
Com o entendimento das ondas eletromagnéticas descobriu – se que os raios X são parte do espectro eletromagnético. As 4 equações de James Clerk Maxwell já haviam demostrado que a luz visível, as ondas de rádio, os raios ultravioletas e os raios X são todos basicamente ondas eletromagnéticas. Mas o que é uma onda?
Vamos começar essa explicação imaginando um elétron que se movimenta no espaço para cima e para baixo, em um movimento cíclico e repetitivo. O elétron possui carga negativa. Com isso, ele é capaz de atrair partículas com cargas positivas, já que cargas opostas se atraem e cargas iguais se repelem.
Agora idealize que esses elétrons estão oscilando na superfície Solar, a aproximadamente 151 milhões de km de distância da Terra. Mesmo sem deixar a superfície do Sol, os elétrons de lá exercem força de repulsão sobre os elétrons que estão nas órbitas dos átomos da sua mão, ainda que essa força seja muito pequena (a Lei de Coulomb pode ser usada para estimar essa força).
Desta forma, quando os elétrons lá na superfície do Sol oscilam, eles conseguem induzir os elétrons da sua mão a se moverem num movimento cíclico. Os elétrons não precisam sair lá do Sol para te bombardear (você não ia querer que isso ocorresse mesmo, rsrs). Eles precisam simplesmente oscilar… E você sentirá essa oscilação, aproximadamente 8 minutos depois…
Não acredita que funciona assim? Tenho certeza de que em um dia quente, você já sentiu sua mão esquentar quando exposta diretamente à luz do Sol. De onde você acha que vem aquela sensação?
Os elétrons podem oscilar lentamente ou mais rápido. O número de oscilações por segundo chamamos de frequência da oscilação. Maxwell, por meio das suas equações, já havia descoberto que a luz viaja a aproximadamente 300.000 km/s. Assim, para que que você sinta a oscilação de alguma carga na superfície do sol, é necessário um tempo de aproximadamente 8 min.
Toda partícula carregada, como os elétrons no nosso exemplo, possui um campo elétrico associada a ela. Se a partícula estiver parada, não temos uma onda se propagando. Mas, se a partícula carregada oscilar de maneira cíclica, como no nosso exemplo, podemos imaginar que esse campo elétrico também deverá oscilar. Faraday e Ampère já haviam demonstrado que é impossível que um campo elétrico oscilante exista sozinho. Ele sempre estará acompanhado de um campo magnético, com mesma frequência, mas perpendicular em relação ao campo elétrico. Assim, sempre que uma partícula carregada oscilar, teremos uma onda eletromagnética.
Outra característica importante de uma onda é seu comprimento de onda (l). O comprimento de onda é a distância que a onda precisa percorrer para completar uma oscilação completa. Ele está diretamente relacionado com a frequência: se a frequência da onda for muito alta, o comprimento de onda ficará muito pequeno (será necessária uma pequena distância para que ciclo se complete). Por outro lado, para oscilações de baixa frequência, o comprimento de onda será, portanto, maior.
Tudo bem! E o que tudo isso tem a ver com os materiais?
Ondas eletromagnéticas com comprimentos de onda entre 400 e 900 nm (lembrando: 1 nanômetro [nm] é 1 metro dividido por um bilhão!) correspondem justamente a luz visível! Isso mesmo. A luz que você, eu e todos nós usamos para enxergar é, na verdade uma parte do espectro eletromagnético.
Os raios X também são parte do mesmo espectro eletromagnético. Eles possuem comprimentos de onda da ordem de 0,1 nm, bem menores que os da luz visível. Veja a Figura 1 que mostra outras partes importante do espectro eletromagnético.
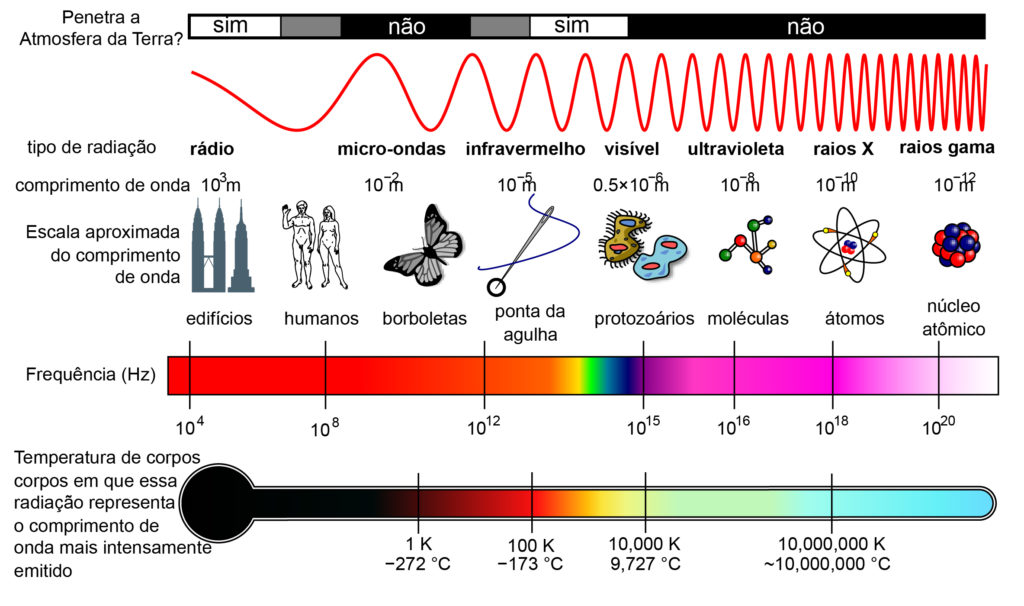
Figura 1 – O espectro eletromagnético
O interessante é que nos materiais, a distância média entre os átomos também é da ordem de 0,1 nm. Os Raios X foram descobertos no final de 1895 pelo físico alemão Wilhelm Konrad Röentgen. Em 1912, Max Von Laue e seus colegas tiveram a ideia de irradiar cristais de sulfeto de cobre com esses novos raios X. E uma coisa muito interessante aconteceu. Veja a Figura 2.
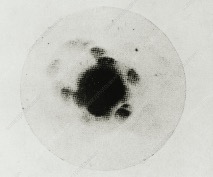
Figura 2 – Primeira difração de Raios X obtida pelo grupo de Max von Laue para cristais de sulfeto de Cobre.
Sim, a imagem está meio borrada. Mas é possível notar pontos claros e escuros na foto. Isso era um indício de que estava ocorrendo dois fenômenos bem característicos das ondas: interferência e difração.
A difração só ocorre quando uma onda colide com um obstáculo que tem um tamanho próximo ao seu comprimento de onda. As ondas geradas por cada obstáculo (no caso dos materiais, os próprios átomos), podem interferir de maneira construtiva ou destrutiva. Tudo depende como elas se “encontram” no espaço: se as ondas estiverem em fase, iríamos observar uma intensificação do sinal (interferência construtiva). Mas caso estivessem fora de fase, elas simplesmente se cancelariam (interferência destrutiva). Os pontos que você vê na imagem são, portanto, regiões onde os raios X interferiram de maneira construtiva. Essa foi uma descoberta de tamanha importância, que von Laue ganhou o prêmio Nobel em 1914. Com seu resultado, von Laue demonstrou que os átomos não estão localizados ao acaso no material. Eles estão organizados num arranjo periódico muito preciso. Se não fosse assim, veríamos simplesmente um borrão difuso.
Importante comentar que a ideia de von Laue não surgiu por acaso. Antes dele, muitos cientistas já desconfiavam que alguns materiais apresentavam átomos dispostos de maneira bem-organizada. Esta era a melhor forma de explicar a formação de cristais de gelo e de alguns minerais na natureza, como os mostrados na Figura 3. A diferença é que von Laue foi o primeiro cientista que conseguiu, de fato, provar que a organização atômica era uma realidade.
 |
 |
|
(a) |
(b) |
Figura 3 – Cristais de Gelo (a) e de Pirita [FeS2], o famoso “ouro de de tolo” (b)
Após a descoberta de von Laue, o campo começou a avançar rapidamente. O físico William Lawrence Bragg descobriu como usar as imagens de difração para calcular as distâncias entre os átomos e a forma como os átomos se organizam no material. Foi o nascimento da Lei de Bragg. Ele e seu pai, Willian Henry Bragg, utilizaram a Lei de Bragg para deduzir a estrutura cristalina do sal de cozinha e, com isso, descobriram as ligações iônicas, por meio da forma como os elétrons se distribuem no material. Desvendaram ainda a estrutura do diamante e de muitos outros materiais. O trabalho dos Bragg foi tão importante que eles receberam o prêmio Nobel um ano após von Laue, em 1915. Graças ao trabalho de von Laue e dos Braggs, foi possível entender que a forma como os átomos se organiza em cada material tem impacto enorme nas usas propriedades. Eles ganharam o prêmio Nobel e ainda possibilitaram o nascimento de um novo campo da ciência: a cristalografia.
A partir dos experimentos dos Braggs, a estrutura cristalina dos cerâmicos iônicos foi desvendada. Depois a estrutura dos metais e por fim, a estrutura dos materiais orgânicos como os polímeros. Até o formato de dupla hélice do DNA só pôde ser descoberto graças à experimentos envolvendo difração de raios X.
Materiais cristalinos, quasicristais e materiais amorfos
A cristalografia mostrou que a maioria dos materiais na natureza são cristalinos. Bravais mostrou que a estrutura cristalina dos materiais pode ser resumida em 14 redes, como mostra a Figura 4.
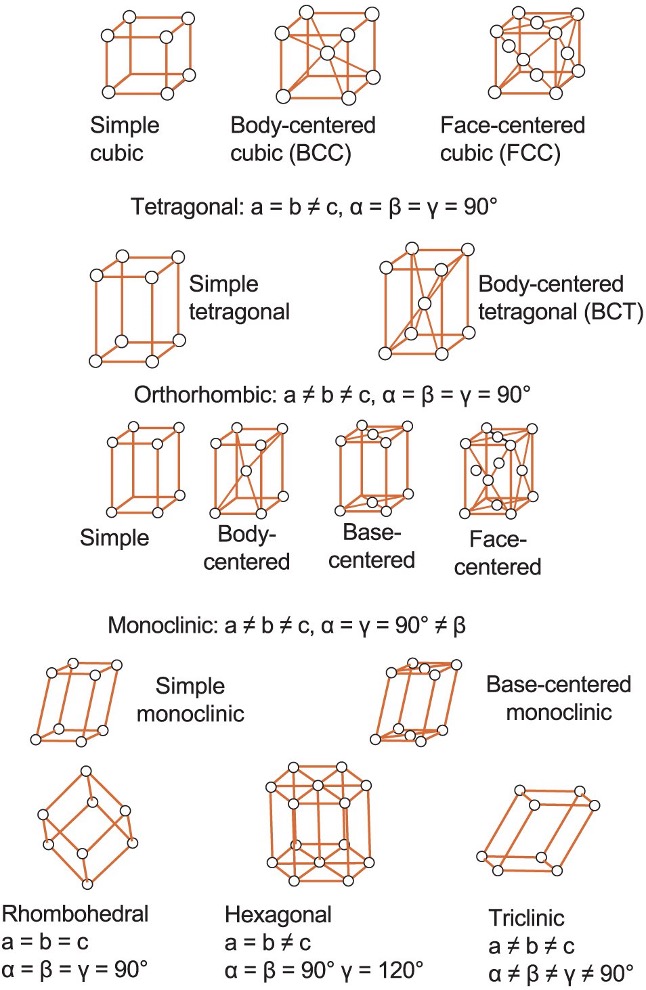
Figura 4 – Redes de Bravais.
Alguns materiais, no entanto, não presentam uma ordem de longo alcance na posição dos átomos da rede. Nesses materiais, as distâncias interatômicas não são bem definidas, mas podem variar bastante de ponto para ponto na rede do material. São os chamados materiais amorfos ou materiais não-cristalinos (na realidade existe uma diferença entre esses materiais, mas discutiremos isso em outro artigo). Os vidros e os polímeros, assim como os vidros metálicos são parte desse interessante grupo.
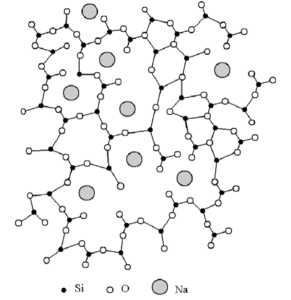
Figura 5 – Representação da rede de um vidro de Sílica.
Existem materiais que exibem ordem de longo alcance, mas numa simetria que desafia as redes de Bravais. Na verdade, até certo tempo, não pensávamos que poderiam existir materiais com estruturas cristalinas diferentes daquelas postuladas por Bravais. Mas eles existem! São os quasicristais, que, com certeza, terão um artigo dedicado somente para eles.

Figura 6 – Imagens da estrutura de um quasicristal. Repare nas faces pentagonais do material.
Aliás um material pode ser composto por um único cristal, como o diamante, ou por múltiplos grãos, cada um com sua orientação cristalográfica, como a maioria dos metais. Assim distinguimos Materiais Monocristalinos de Materiais Policristalinos, como mostra a Figura 7.
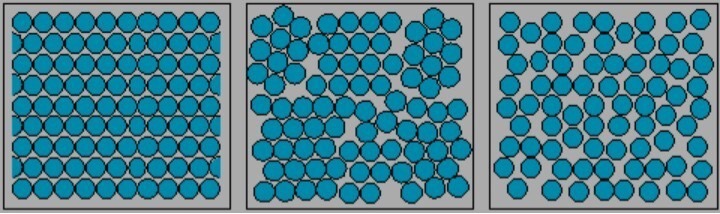
Figura 7 – Representação de um monocristal (à esq.), de um material policristalino (ao meio) e de um material amorfo (à dir.).
Ainda hoje, usamos raios X para desvendar a estrutura de novos materiais, fármacos e por aí vai. Com esses resultados conseguimos entender melhor como produzir e processar materiais melhores e até compreender como as proteínas se dobram e como seria possível produzir remédios mais eficazes.
Esse artigo já ficou grande, por isso continue ligado no site para mais. E se você tiver algum assunto que queira ver por aqui, fale com a gente nas redes sociais! Até a próxima!
Fontes das Imagens:
Khemis, https://commons.wikimedia.org/w/index.php?curid=41541569
How ice crystals form in clouds, https://analyticalscience.wiley.com/do/10.1002/micro.2104
Friedrich, W., Knipping, P e Laue, M. von,; Ann. Phys. 41 (1913) 971
Pirita, https://pt.wikipedia.org/wiki/Pirita
Abou Sharma et al. / Journal of Non-Crystalline Solids 353 (2007) 2708–2716
Quasicristais, https://www.jornalciencia.com/quasicristal-raro-e-encontrado-em-meteorito-que-caiu-na-russia/
https://www.feis.unesp.br/Home/departamentos/engenhariamecanica/maprotec/historico_raios_x.pdf

